第23届全国临床肿瘤学大会暨2020年CSCO学术年会采取线上+线下同步直播的方式于2020年9月19日~9月26日在北京等五地成功举行。乳腺癌专场上,来自天津医科大学肿瘤医院的郝春芳教授做出了“晚期乳腺癌内分泌治疗新组合新靶点”的报告,现整理如下,以飨读者。
纵观晚期乳腺癌内分泌治疗历程,新的药物出现不断引领着这一领域治疗的变革,HR+晚期乳腺癌进入靶向治疗新时代。随着治疗药物越来越多,内分泌治疗的战线越来越长,内分泌治疗耐药后的研究越来越精准,内分泌治疗和化疗/其他靶向治疗药物间的适时转换越来越复杂。此外,HR+/HER2-晚期乳腺癌靶向治疗时代一个突出的特点是多靶点、多组合。
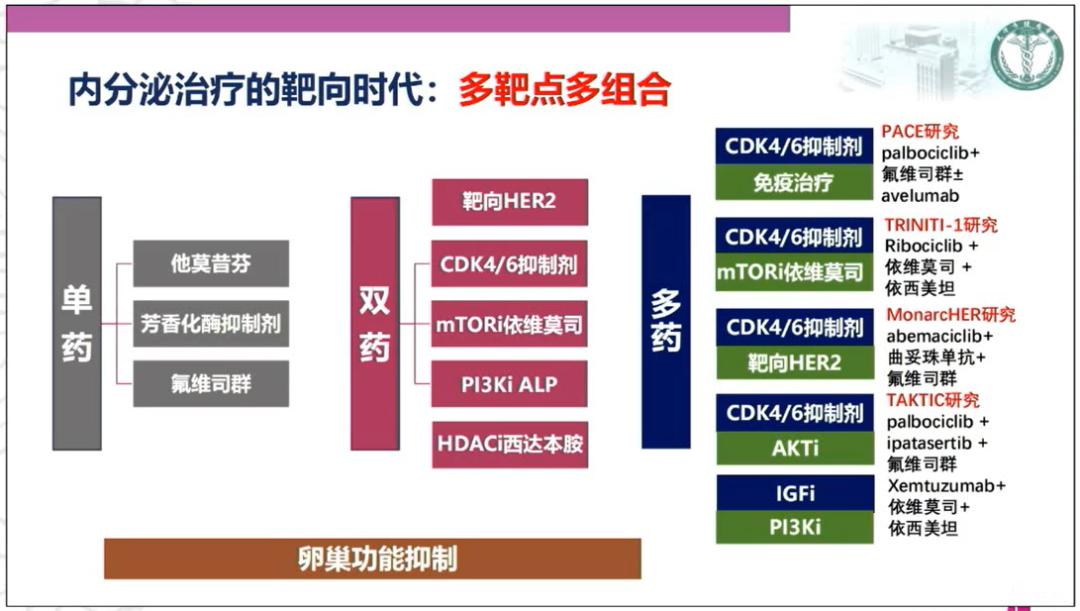
从经典的他莫昔芬、芳香化酶抑制剂以及氟维司群等单药治疗到联合靶向抗HER2治疗药物、CDK4/6抑制剂、mTOR抑制剂、PI3K抑制剂以及HDAC抑制剂西达本胺的治疗,HR+/HER2-晚期乳腺癌患者内分泌治疗和靶向治疗取得了突破性进展,并不断更新着HR+乳腺癌的治疗理念。如今,针对内分泌治疗耐药患者进行的多药联合研究也正在进行中,如CDK4/6抑制剂联合氟维司群及免疫治疗(PACE研究);CDK4/6抑制剂联合依维莫司及依西美坦(TRINITI-1研究);CDK4/6抑制剂联合曲妥珠单抗及氟维司群(MonarcHER研究)以及IGF抑制剂Xentuzumab+依维莫司+依西美坦等多药联合治疗等。
面对如此繁杂的治疗选择,如何对HR+晚期乳腺癌治疗进行合理的排兵布阵也是临床医生面临的一大难题。
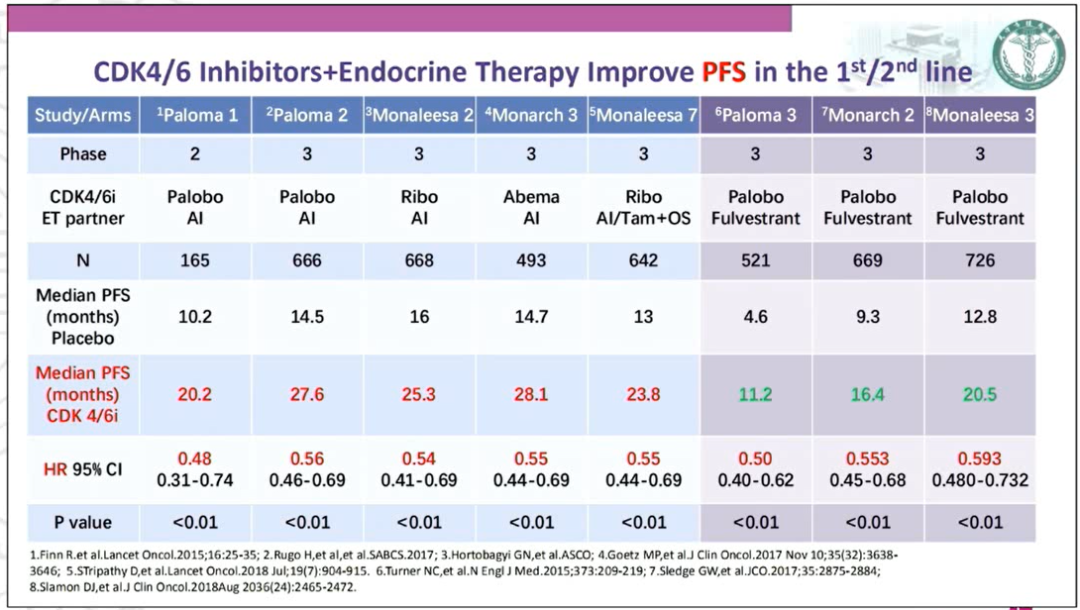
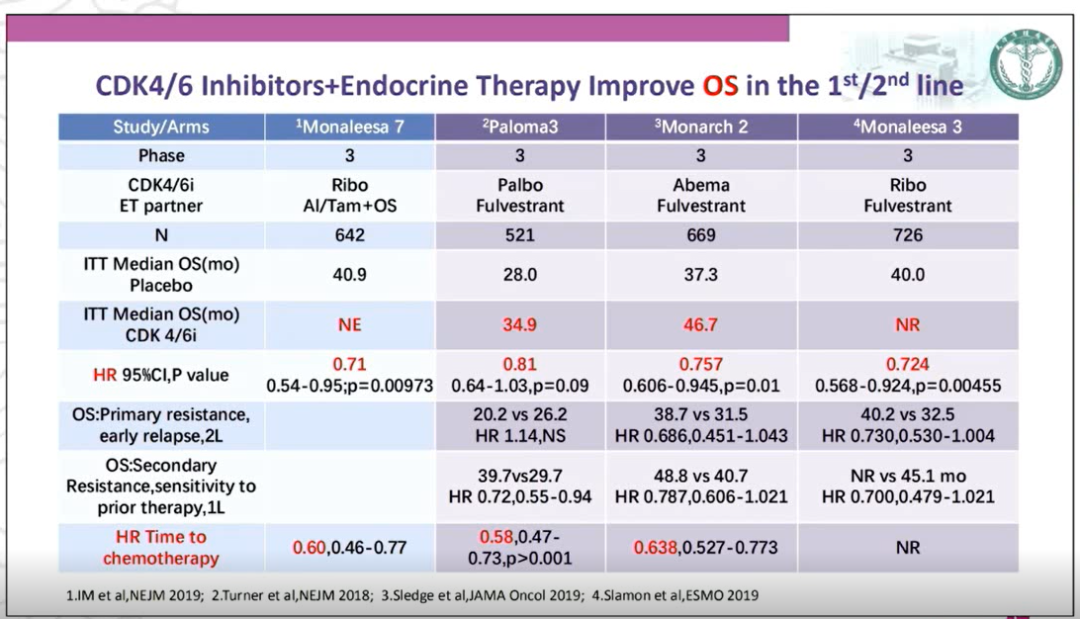
2020版CSCO BC指南其进行了明确的推荐,其中CDK4/6抑制剂的联合治疗方案作为HR+晚期乳腺癌一线、二线内分泌治疗的优选。对于绝经后HR+晚期乳腺癌治疗,如果既往未使用过内分泌治疗,则Ⅰ级推荐为AI+CDK4/6抑制剂(1A);既往TAM治疗失败的患者,Ⅰ级推荐为AI+CDK4/6抑制剂(1A)和氟维司群+CDK4/6抑制剂(1B);(非)甾体类AI治疗失败,Ⅰ级推荐为氟维司群+CDK4/6抑制剂(1A)。其循证医学的证据主要来自于PALOMA、MONALEESA以及MONARCH系列研究,这些均证实CDK4/6抑制剂联合AI在HR+/HER2-晚期乳腺癌的疗效显著优于单药AI或氟维司群:在一线治疗的PFS可以达到20.2~28.1个月,显著降低45%~52%的复发风险,二线治疗中PFS为11.2~20.5个月,也能够降低50%的复发风险(以上数据P值均小于0.01),其中一些研究报告的ITT人群OS的结果更是长达40多个月。此外,在评价至化疗的时间(Time to chemotherapy)上也看到了CDK4/6抑制剂联合治疗的获益。
新药物联合方案获益带来新的问题:
1、在CDK4/6抑制剂联合治疗疗效如此好的大背景下,一线内分泌单药治疗的地位如何?优选人群有哪些?
尽管一线治疗中CDK4/6抑制剂治疗是优选,但是目前CDK4/6抑制剂还未进入我国医保目录,因此临床普及率不是很高,单药治疗对大部分患者来说还是重要选择。ABC5指南投票中专家组一致推荐,如果患者一线治疗中CDK4/6抑制剂治疗不可及,患者转移负荷(转移的数量和部位)不重且生物学特性不太具有侵袭性(比如DFI很长),可以考虑单药内分泌治疗。目前尚没有准确识别单药或者联合治疗优势人群的生物标志物。
2、CDK4/6抑制剂的biomarker?(疗效预测指标)
2020年ASCO大会报道了循环肿瘤DNA(ctDNA)帮助筛选内分泌治疗耐药的指标,即基于MONALEESA试验中进行ctDNA分析进行预测CDK4/6抑制剂疗效潜在生物标志物的汇集分析的结果,发现CHD4、CDKN2A/B/C等基因突变可能是潜在的预测ribociclib联合内分泌治疗耐药的指标,但是对内分泌治疗的疗效没有影响。因此,目前筛选内分泌治疗最重要的biomarker仍然还是ER,在其他生物标志物的探索上期待未来结果的发布。
中国方案中国智造:除了刚刚提到的CDK4/6抑制剂,在2020版CSCO BC指南中还体现了中国方案:对于绝经后HR+/HER2-患者和TAM/非甾体类AI治疗失败的患者还推荐西达本胺联合内分泌治疗,ACE研究证实西达本胺联合依西美坦的疗效显著优于安慰剂联合依西美坦,即对于既有耐药因素又有内脏转移相对难治因素的患者西达本胺的确是一种选择。
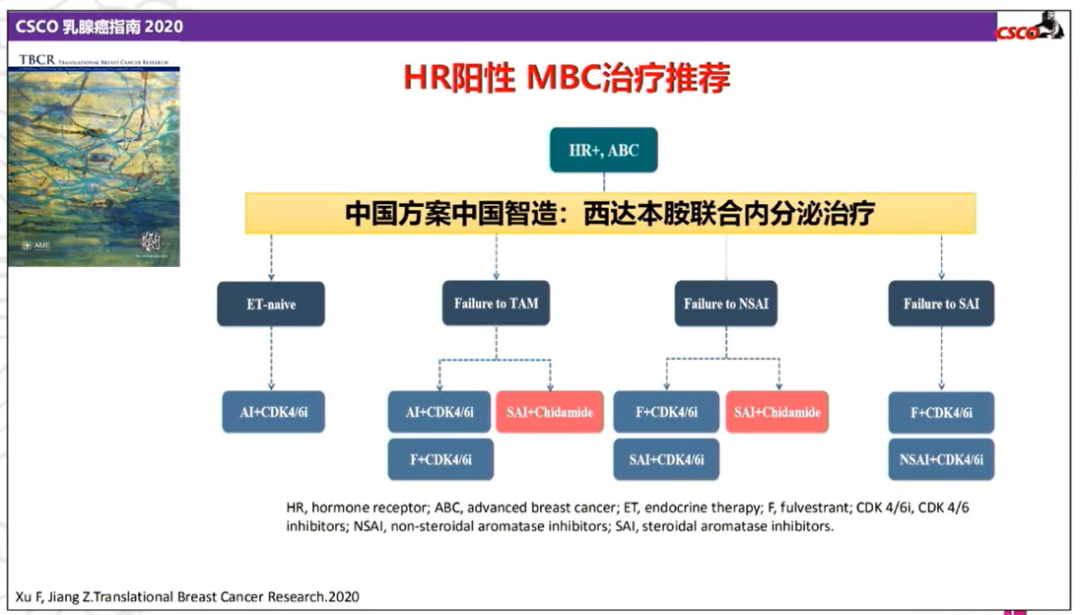
在HR+晚期乳腺癌二线+靶向联合内分泌治疗的研究中,基本上是以氟维司群为基础再联合其他不同作用靶点的药物,如联合CDK4/6抑制剂、PI3K抑制剂、mTOR抑制剂、AKT抑制剂等,相对于氟维司群单药,靶向联合内分泌治疗的联合治疗方案均显著改善了患者PFS。
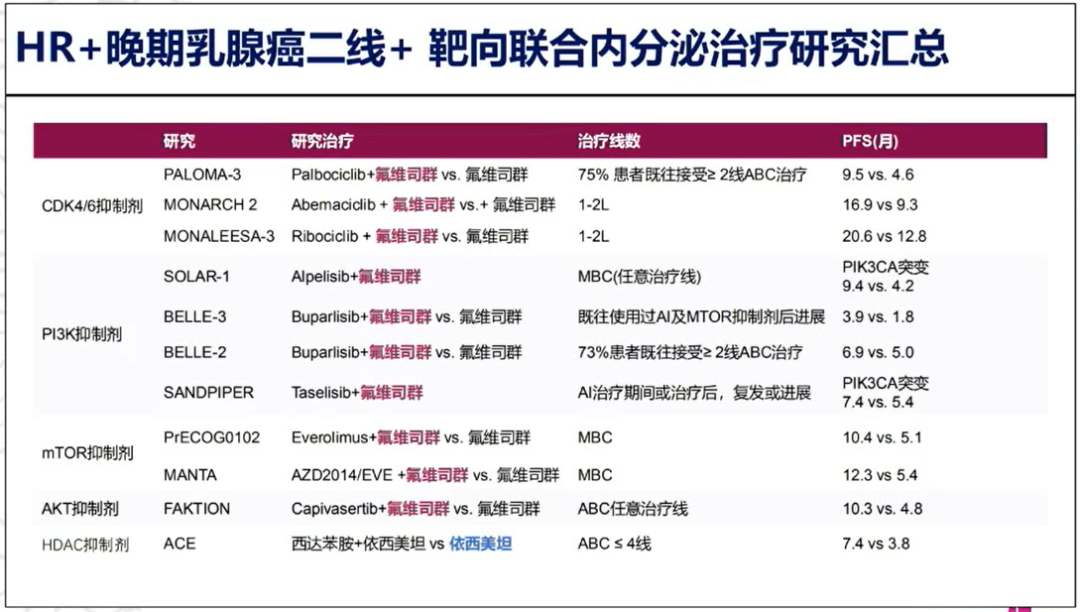
CDK4/6抑制剂耐药机制包括HDAC激活,PI3K/AKT/mTOR通路亚组过表达等,有研究也进行了其他靶点治疗药物的探索,SOLAR-1研究显示了Alpelisib在PIK3CA突变的内分泌治疗耐药在HR+/HER2-晚期乳腺癌中取得了良好的治疗效果。2020年ASCO报道的BYLieve作为第一个专注于CDK4/6抑制剂治疗后进展且合并PIK3CA突变的HR+/HER2-晚期乳腺癌的研究,该研究达到主要终点:6个月无疾病进展的比例为50.4%(95%CI: 41.2%~59.6%),次要研究终点中位PFS也达到了7.3个月。
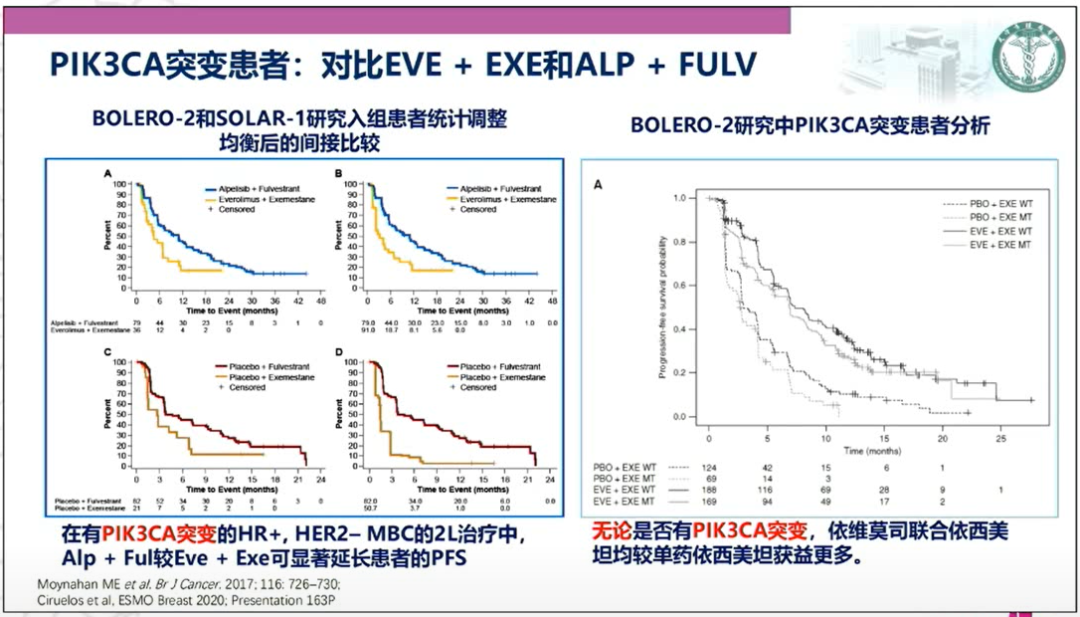
针对PI3K/Akt/mTOR通路的mTOR抑制剂依维莫司,在BOLERO-2研究中显示无论是否存在PIK3CA突变,依维莫司联合依西美坦较单药依西美坦均能给内分泌治疗失败的HR+晚期乳腺癌患者带来临床获益。目前尚没有针对PIK3CA突变患者进行依维莫司+依西美坦和Alpelisib+氟维司群头对头直接的比较的临床试验,将BOLERO-2和SOLAR-1研究入组患者统计调整均衡后的间接比较显示,在有PIK3CA突变的HR+/HER2-转移乳腺癌患者的二线治疗中,Alpelisib+氟维司群较依维莫司+依西美坦可显著延长PFS。
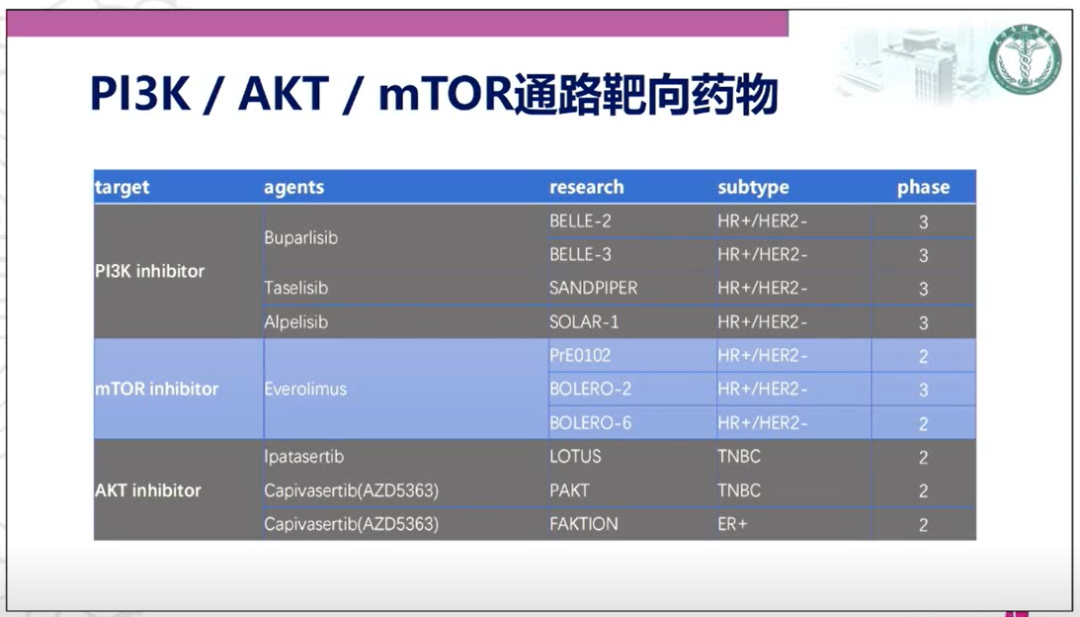
目前针对PI3K/Akt/mTOR通路靶向药物的临床研究有很多,不断丰富着内分泌治疗耐药患者的治疗策略。NCCN指南推荐对于HR+/HER2-转移乳腺癌耐药患者,应该进行相关基因检测,根据相应靶点选择精准治疗药物。
?
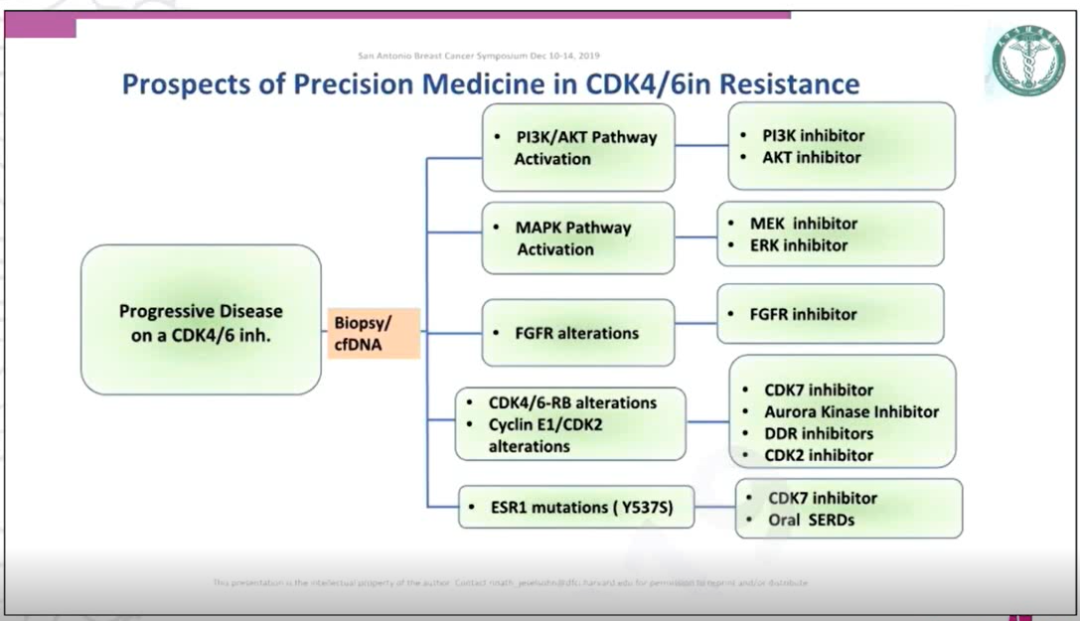
目前针对多个相关靶点药物的研究正在进行中,如FGFR抑制剂、MEK抑制剂、CDK2抑制剂以及CDK7抑制剂等。整体来看HR+晚期乳腺癌进入到了靶向治疗新时代,拓宽了内分泌治疗的“敏感”人群。优化治疗顺序可以延长内分泌治疗敏感性,减缓疾病进展,推迟至化疗的时间。目前一线治疗有多种选择,既有内分泌治疗和化疗之争,内分泌治疗领域又存在单药和联合之争,进入联合内分泌治疗时代后,又有联合配伍药物之争;二线治疗已全线进入了内分泌治疗联合靶向治疗的时代;三线内分泌治疗在联合治疗基础之上更加考虑靶点的检测,根据相应靶点精准选择联合治疗药物。对于HR+难治性晚期乳腺癌,适时转换化疗,化疗后可考虑维持内分泌治疗。
总之,HR+/HER2-晚期乳腺癌治疗需要考虑既往内分泌治疗无病间期、内分泌治疗反应、肿瘤负荷以及是否存在需要快速控制的症状等临床参数,也要考虑到患者年龄、体能状态、合并疾病、社会经济学和心理学等患者相关因素。希望通过合理选择、有序安排、全程管理和精准决策,努力把每一个优效方案用到最佳!
天津医科大学肿瘤医院乳腺内科副主任医师、医学博士
中国抗癌协会乳腺癌专业委员会青委会副主任委员
中国临床肿瘤学会(CSCO)乳腺癌专家委员会委员
中国临床肿瘤学会(CSCO)青年专家委员会常务委员
中国医药教育协会乳腺疾病专业委员会委员
北京乳腺病防治学会健康管理专业委员会常务委员
北京乳腺病防治学会国际医疗与合作专业委员会常务委员





 京公网安备 11010502033352号
京公网安备 11010502033352号